Le chlorite de sodium : une alternative controversée et dangereuse pour le blanchiment dentaire
Le chlorite de sodium, composé chimique de formule NaClO₂, émerge depuis quelques années comme un agent blanchissant dentaire alternatif, particulièrement dans les produits de vente libre non réglementés. Contrairement aux peroxydes bien établis (peroxyde d’hydrogène et carbamide) et au PAP innovant, le chlorite de sodium représente une voie largement controversée en dentisterie esthétique. Son mode d’action unique — la génération de dioxyde de chlore dans l’environnement acide de la bouche — offre certains avantages en termes de blanchiment rapide, mais s’accompagne de risques biologiques significatifs et insuffisamment compris. Cet article examine en détail le chlorite de sodium, son historique en dentisterie, son mécanisme d’action chimique complexe, les données comparatives limitées disponibles, et surtout les préoccupations sérieuses concernant sa sécurité pour la santé bucco-dentaire.
Historique et contexte : L’émergence d’une substance ancienne en dentisterie moderne
Découverte du chlore et de ses dérivés
Le chlorite de sodium ne peut être dissocié de l’histoire plus large du chlore lui-même. Le chlore élémentaire (Cl₂) a été découvert en 1774 par le chimiste suédois Carl Wilhelm Scheele en faisant réagir du dioxyde de manganèse (MnO₂) avec de l’acide chlorhydrique (HCl). Le composé gazeux vert pâle obtenu n’a été formellement identifié comme un élément distinct que 36 ans plus tard, en 1810, par le chimiste britannique Humphry Davy, qui lui a donné le nom « chlore » (du grec ancien χλωρός, khloros, signifiant « vert pâle »). À partir de ce moment, le chlore et ses dérivés — hypochlorite, chlorite, chlorate — se sont multipliés dans les applications industrielles et médicales.
Production industrielle du chlorite de sodium
Le chlorite de sodium en tant que sel stable a été synthétisé initialement en réagissant le dioxyde de chlore (ClO₂) avec de l’hydroxyde de sodium (NaOH), produisant un mélange contenant du chlorite de sodium (NaClO₂) et du chlorate de sodium (NaClO₃). La synthèse directe de chlorite pur requiert des étapes supplémentaires, particulièrement l’addition de peroxyde d’hydrogène pour éliminer le chlorate contaminant. Cette production relativement complexe a longtemps limité la disponibilité du composé.
Le développement du procédé Mathieson, breveté en 1950 aux États-Unis par Diamond Alkali Co, a révolutionné la production de chlorite de sodium pur en grande quantité. Le procédé utilise le dioxyde de chlore généré in situ réagissant avec l’hydroxyde de sodium ou du carbonate de sodium, optimisant la sélectivité pour le chlorite. À partir de cette période, le chlorite de sodium est devenu largement disponible pour des applications industrielles majeures : blanchiment de papier et textile, désinfection de l’eau potable, traitement des eaux usées, et applications alimentaires.
Émergence récente en dentisterie esthétique
L’utilisation du chlorite de sodium pour le blanchiment dentaire est extrêmement récente, remontant seulement aux années 2010 et gagnant en popularité après 2015. Contrairement aux peroxydes avec un historique de plus d’un siècle en dentisterie, et le PAP avec des études depuis 2017-2018, le chlorite de sodium en applications dentaires bénéficie d’une base de données scientifiques remarquablement limitée.
L’apparition du chlorite de sodium dans des kits de blanchiment OTC (over-the-counter) reflète largement les restrictions réglementaires européennes de 2012 limitant les concentrations de peroxyde d’hydrogène dans les produits de vente libre. Face à ces restrictions, certains fabricants se sont tournés vers des alternatives chimiques moins réglementées, dont le chlorite de sodium. Malheureusement, cette transition vers le chlorite de sodium s’est opérée sans accumulation préalable suffisante de données de sécurité clinique.
Structure chimique et propriétés moléculaires fondamentales
Composition et caractérisation chimique
Le chlorite de sodium possède une formule chimique simple : NaClO₂. Il s’agit d’un sel blanc cristallin, inodore, légèrement soluble dans l’eau (640 g/L à 17°C). À l’état solide pur, le chlorite de sodium anhydre cristallise dans le système monoclinique avec des paramètres de maille spécifiques. Le composé commercial se présente généralement en solution aqueuse stabilisée, typiquement à des concentrations de 25% ou 31%.
La structure moléculaire révèle l’anion chlorite (ClO₂⁻) interagissant ioniquement avec le cation sodium (Na⁺). L’anion chlorite possède une géométrie de V amide avec le chlore au sommet et les deux atomes d’oxygène positionnés symétriquement. Cette structure confère au composé ses propriétés chimiques distinctives : stabilité relative en solutions neutres à alcalines, mais réactivité extrême en environnement acide.
Distinction chimique critique : NaClO₂ vs. NaClO
Confusion fréquente : le chlorite de sodium (NaClO₂) ne doit absolument pas être confondu avec l’hypochlorite de sodium (NaClO), communément connu sous le nom d’eau de Javel. Bien que l’hypochlorite soit largement utilisé en désinfection dentaire (notamment en traitement des canaux radiculaires), ses propriétés biologiques et ses applications diffèrent fondamentalement du chlorite de sodium. L’hypochlorite possède un pouvoir désinfectant supérieur mais une stabilité inférieure. Le chlorite de sodium, par contraste, demeure plus stable en stockage mais génère le dioxyde de chlore hautement réactif quand activé.
Mécanisme d’action : génération de dioxyde de chlore et oxydation des chromophores
Activation acide et production de dioxyde de chlore
Le cœur du système de blanchiment au chlorite de sodium repose sur son activation chimique. En environnement neutre ou légèrement alcalin, le chlorite de sodium demeure relativement inactif et stable. Cependant, au contact d’un acide — particulièrement l’acide citrique couramment ajouté aux produits commerciaux — une réaction exothermique s’enclenche.
La réaction chimique peut être représentée de manière simplifiée : NaClO₂ + HCl (ou acide citrique) → ClO₂ + NaCl + H₂O.
Le dioxyde de chlore (ClO₂) généré constitue l’agent actif principal responsable du blanchiment. Le dioxyde de chlore est un gaz jaune-vert hautement réactif et instable — exactement le même composé utilisé comme désinfectant dans les systèmes de traitement d’eau municipale et, remarquablement, comme agent de désinfection des piscines.
Efficacité blanchissante par oxydation directe
Une fois généré, le dioxyde de chlore agit comme un puissant oxydant, attaquant les structures moléculaires responsables de la coloration dentaire. Le mécanisme dépasse largement la simple oxydation des chromophores : le dioxyde de chlore attaque directement la matrice organique de l’émail et de la dentine, fragmentant les protéines et les polysaccharides structuraux.
Cette oxydation non-sélective crée plusieurs conséquences importantes.
Premièrement, elle produit l’effet blanchissant recherché via la destruction des pigments responsables de la coloration.
Deuxièmement, cependant, cette même puissance oxydante endommage simultanément les constituants bénéfiques de la structure dentaire elle-même. Contrairement au PAP qui transfère sélectivement un atome d’oxygène aux chromophores via époxidation (un mécanisme chimique distinct), le chlorite de sodium engendre une oxydation diffuse et non spécifique.
Conditions d’acidité déterminantes
Un paramètre critique influençant l’efficacité du chlorite de sodium concerne le pH de l’environnement buccal. Le chlorite de sodium génère des quantités significatives de dioxyde de chlore seulement dans des conditions acides (pH < 7, idéalement < 5). Certains produits commerciaux contiennent de l’acide citrique précisément pour créer cet environnement acide optimisant la génération de dioxyde de chlore.
Hélas, l’acide citrique lui-même présente un problème dentaire major : l’acide citrique est un puissant érodant de l’émail dentaire. À des pH inférieurs à 5,5, l’émail commence à se déminéraliser significativement. Donc, les formulations commerciales optimisant techniquement la génération de dioxyde de chlore le font précisément au prix de créer des conditions d’acidité corrosives pour l’émail lui-même.
Efficacité blanchissante : données comparatives limitées et problématiques
Résultats d’études comparatives : chlorite vs peroxydes et PAP
Une étude in vitro majeure de 2023 a directement comparé l’efficacité blanchissante de plusieurs agents : peroxyde d’hydrogène, peroxyde de carbamide, PAP, bicarbonate de sodium, bromélaïne, et chlorite de sodium. L’étude impliquait 60 dents humaines extraites, tachées à l’aide de café, puis exposées durant 7 jours à chacun des agents blanchissants.
Les résultats, mesurés sur l’échelle CIELAB (ΔE) — où des valeurs supérieures à 3,7 indiquent un changement cliniquement perceptible — révélaient :
- Peroxyde d’hydrogène : ΔE = 9,6 (p < 0,001) — le plus efficace
- Bicarbonate de sodium : ΔE = 7,5 (p < 0,001)
- PAP : ΔE = 6,6 (p < 0,01)
- Bromélaïne : ΔE = 5,3 (non significatif)
- Chlorite de sodium : ΔE = 3,9 (non significatif)
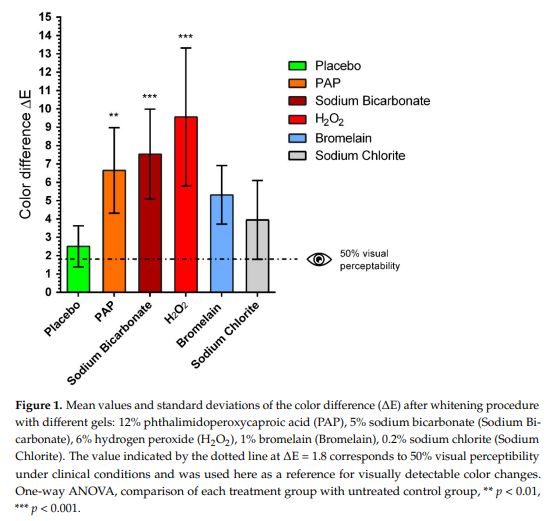
Le chlorite de sodium échoue à atteindre la significativité statistique et son ΔE de 3,9 représente à peine le seuil de perceptibilité clinique (3,7). En d’autres termes, le blanchiment au chlorite de sodium dans cette étude rigoureuse demeurait en dessous du seuil de détection visuelle pour la moitié environ de la population. Comparé au peroxyde d’hydrogène (ΔE = 9,6), le chlorite de sodium offrait une efficacité inférieure de 59%.
Distinction critique : élimination des taches vs. véritable blanchissement
L’étude précédente révélait une distinction nuancée mais cruciale. Le peroxyde d’hydrogène blanchissait les dents au-delà de leur teinte naturelle initiale, passant par l’élimination des taches puis l’oxydation supplémentaire de la structure dentaire naturelle. Par contraste, le chlorite de sodium ne parvenait qu’à éliminer les taches extrinsèques de surface (la couche de café appliquée) sans produire de véritable blanchissement intrinsèque.
Cela signifie qu’un patient ayant des taches modérées de surface (café, vin, tabac) observerait potentiellement un résultat cosmétique, tandis que celui ayant des colorations intrinsèques profondes (jaunissement lié à l’âge, medicaments, traumatismes) constaterait un résultat décevant voire imperceptible.
Efficacité insuffisante pour les applications cliniques sérieuses
En contexte clinique, l’efficacité insuffisante du chlorite de sodium soulève des questions sérieuses concernant son utilité. Les patients attendant un blanchiment cosmétiquement significatif risquent une déception majeure, particulièrement étant donné les risques associés (détaillés ci-dessous).
Inconvénients et effets indésirables significatifs
Altération irréversible de l’émail
Le problème majeur du chlorite de sodium — particulièrement lorsqu’il est formulé avec de l’acide citrique comme « accélérateur » — concerne son potentiel destructeur pour l’émail dentaire. L’acide citrique ramollit et dissout progressivement l’émail via une réaction de déminéralisation.
Une étude britannique publiée dans le British Dental Journal a évalué cinq kits de blanchiment OTC populaires vendus en ligne, révélant que quatre contenaient de l’acide citrique associé au chlorite de sodium. Les résultats cliniques observés chez les utilisateurs incluaient une érosion progressive de l’émail, initialement imperceptible, mais s’accumulant avec les applications répétées.
L’aspect profondément problématique réside dans l’irréversibilité : une fois que l’émail est dissous et érodé, il ne peut jamais se régénérer. Bien que la dentine sous-jacente puisse se reminéraliser grâce à la salive et aux applications de fluorure, l’émail érodé demeure définitivement perdu. Cette perte progressive de l’émail protecteur crée une cascade de problèmes : exposition dentinaire, sensibilité chronique, susceptibilité accrue aux caries, et au fil du temps, jaunissement progressif des dents — ironiquement, l’exact opposé du résultat recherché.
Ironie paradoxale : recoloration accélérée et jaunissement à long terme
Une conséquence remarquable et perverse de l’utilisation du chlorite de sodium émerge avec le temps : les patients constatent une recoloration plus rapide et plus marquée que celle observée après blanchiment professionnel classique. Cette recoloration accélérée s’explique : une fois l’émail protecteur endommagé, la dentine jaune sous-jacente s’expose progressivement aux éléments, se colorant facilement aux aliments, boissons, et tabac. Le résultat esthétique net, après quelques mois, devient pire qu’avant le traitement initial.
Brûlures chimiques et lésions gingivales
Le chlorite de sodium et son produit de décomposition, le dioxyde de chlore, causent des brûlures chimiques graves au contact des muqueuses buccales — gencives, lèvres, langue, parois intérieures des joues. Ces brûlures chimiques ne sont pas simplement transitoires : selon la concentration et la durée d’exposition, elles peuvent progresser vers des ulcérations, des saignements, voire une nécrose tissulaire localisée.
Un témoignage clinique documenté relate le cas d’une patiente ayant utilisé un kit de blanchiment contenant du chlorite de sodium, qui a développé des ulcérations étendues de la muqueuse buccale, une inflammation gingivale marquée, et une douleur intraitable nécessitant une intervention dentaire d’urgence pour arrêter l’application du produit.
Des brûlures chimiques des gencives posent un risque supplémentaire : une récession gingivale progressive, augmentant le risque à long terme de déchaussement des dents et de perte dentaire.
Sensibilité dentaire prolongée et irréversibilité potentielle
Contrairement au PAP qui produit une sensibilité négligeable et temporaire, ou au peroxyde d’hydrogène qui entraîne une sensibilité transitoire de 24-48 heures, le chlorite de sodium peut produire une sensibilité dentaire chronique et potentiellement permanente. Cette sensibilité résulte de l’exposition progressive des tubuli dentinaires suite à l’érosion de l’émail.
Dans les cas sévères, la dégradation de l’émail est tellement extensive que le nerf dentaire lui-même peut être irrité chroniquement, produisant une hypersensibilité dentaire persistante même après cessation de l’utilisation du produit.
Toxicité systémique potentielle et préoccupations de santé générale
Bien que l’utilisation topique du chlorite de sodium pour blanchir les dents implique surtout des expositions locales, les recherches concernant l’ingestion accidentelle du chlorite de sodium révèlent un profil toxicologique préoccupant à l’échelle systémique.
Une étude française du Centre d’Antipoison suite aux alertes gouvernementales concernant le « MMS » (Miracle Mineral Solution, essentiellement du chlorite de sodium + acide citrique) a documenté : vomissements, fièvre, douleurs gastriques et thoraciques, brûlures graves des muqueuses de l’œsophage et de l’estomac, et troubles sanguins incluant une anémie hémolytique et une atteinte de l’hémoglobine.
Bien que ces effets systémiques majeurs interviennent surtout avec ingestion interne, le potentiel de micro-ingestion accidentelle durant le blanchiment dentaire (patient avalant une portion mineure de gel) soulève des questions concernant la sécurité cumulative, particulièrement chez les enfants ou adolescents.
Manque de données cliniques à long terme
Un inconvénient ultime concerne l’absence quasi-complète de données cliniques à long terme. Tandis que les peroxydes dentaires bénéficient de décennies d’études cliniques multicentriques, et le PAP d’au moins 5-7 années de suivi, le chlorite de sodium pour applications dentaires dispose d’environ 3-4 années de données cliniques seulement, et celles-ci demeurent fragmentaires et limitées.
Les véritables impacts à long terme — notamment sur la progression de la récession gingivale, l’évolution de l’hypersensibilité, et les effets de la minéralisation au fil du temps — demeurent largement inconnus.
Réglementation et statut juridique singulier
L’absence de réglementation dentaire spécifique
Contrairement aux peroxydes (régulés par la Directive EU 2011/84/UE) et au PAP (souvent classé par défaut dans une catégorie cosmétique générale), le chlorite de sodium pour blanchiment dentaire existe dans une zone réglementaire grise remarquablement peu encadrée.
Le chlorite de sodium est approuvé par les autorités sanitaires (notamment la FDA) pour certaines applications désinfectantes alimentaires et de traitement d’eau. Cependant, cette approbation ne s’étend explicitement pas au blanchiment dentaire cosmétique.
En conséquence, les produits contenant du chlorite de sodium pour blanchiment dentaire circulent largement dans un vide réglementaire, vendus en ligne et dans certains magasins de santé sans supervision dentaire, sans contrôle de concentration, et souvent sans mention explicite de la présence de chlorite de sodium sur l’étiquette.
Compositions cachées et manque de transparence
Un problème additionnel grave concerne la transparence des formulations commerciales. Une étude systématique des produits OTC révélait que certains kits contiennent des composants toxiques non listés sur l’étiquette produit. Le chlorite de sodium, l’hexamétaphosphate de sodium, le carbopol, et d’autres substances dangereuses apparaissaient sans disclosure adéquat.
Cette opacité deliberate (ou par négligence) constitue un danger patient significatif. Un utilisateur ne peut pas faire un choix éclairé s’il ignore quels ingrédients actifs se trouvent véritablement dans le produit qu’il applique dans sa bouche.
Recommandations professionnelles contre
Les organisations dentaires majeures — British Dental Association, American Dental Association, et leurs équivalents européens — s’opposent explicitement à l’utilisation du chlorite de sodium pour blanchiment dentaire en raison du profil risque-bénéfice défavorable.
La British Dental Association a déclaré que certains kits contenant du dioxyde de chlore (généré à partir du chlorite) « obtiennent l’effet blanchissant en attaquant la surface de la dent », ce qui « détruit efficacement l’émail protecteur, rendant les dents très sensibles ». L’organisation note que « dans de nombreux cas, les changements sont permanents — dans les cas extrêmes, ils peuvent entraîner la perte des dents ».
Coûts et accessibilité économique
Tarification des produits OTC
Les kits de blanchiment contenant du chlorite de sodium, vendus en ligne, s’affichent généralement à des prix particulièrement attractifs : 20€ à 80€ pour des traitements complets, significativement moins chers que les traitements professionnels (400€-1200€).
Ce prix attractif constitue paradoxalement un facteur de danger : le prix bas incite les patients à ignorer les préoccupations de sécurité, percevant le coût minime comme une couverture contre les risques potentiels. Une patient pensant « c’est bon marché, quoi qu’il en soit, un blanchiment échoué ne me coûtera pas cher » oublie que les dégâts irréversibles à l’émail n’ont pas de « prix de remplacement ».
Absence de remboursement
Comme tous les blanchiments cosmétiques, aucune assurance-maladie ni mutuelle ne rembourse les produits de blanchiment au chlorite de sodium. Cette absence de couverture rend attrayant le prix OTC bas, mais augmente le risque patient du fait de l’absence de supervision professionnelle.
Perspectives d’avenir et trajectoire probable
Probable réglementation croissante
À mesure que les données de sécurité s’accumulent et que les alertes sanitaires se multiplient, une réglementation plus stricte du chlorite de sodium pour blanchiment dentaire est hautement probable. Les autorités sanitaires européennes et nord-américaines s’orientent probablement vers une interdiction complète ou une restriction sévère de son utilisation dans les produits de blanchiment OTC.
Remplacement par des alternatives plus sûres
À mesure que le profil de risque du chlorite de sodium devient mieux compris, les formulateurs se tournent davantage vers des alternatives plus sûres : PAP, enzymes protéolytiques (bromélaïne), et nanoparticules innovantes.
Avenir peu prometteur
Contrairement au PAP qui s’oriente vers une utilisation croissante et une adoption professionnelle, la trajectoire du chlorite de sodium en dentisterie esthétique s’oriente probablement vers une marginalisation progressive et éventuelle disparition du marché professionnel.
Conclusion
Le chlorite de sodium représente un exemple caricatural de ce qui peut survenir quand des innovations chimiques industrielles (les dérivés du chlore) sont imprudemment adaptées à des applications cosmétiques sans accumulation préalable de données de sécurité rigoureuses. Bien que techniquement capable de produire une certaine décoloration dentaire par génération de dioxyde de chlore hautement réactif, le chlorite de sodium offre une efficacité blanchissante décevante (ΔE = 3,9, inadéquat comparé à 9,6 pour le peroxyde d’hydrogène) combinée à des risques biologiques substantiels et insuffisamment compris.
L’association fréquente du chlorite de sodium avec l’acide citrique « accélérateur » crée un double problème : une génération optimisée de dioxyde de chlore couplée à une acidité dentale destructrice. Le résultat clinique à long terme est prévisible : émail progressivement érodé, sensibilité dentaire chronique, recoloration accélérée, et paradoxalement, des dents plus tachées et plus jaunes qu’avant le traitement initial.
Tandis que le peroxyde d’hydrogène s’appuie sur décennies d’études cliniques établissant son profil risque-bénéfice acceptable, que le peroxyde de carbamide offre des résultats prévisibles et durables, et que le PAP émerge comme une alternative novice mais hautement prometteuse, le chlorite de sodium demeure une expérience chimique hasardeuse sans données cliniques robustes pour justifier son utilisation.
Les organisations dentaires professionnelles majeures s’opposent explicitement à l’utilisation du chlorite de sodium pour blanchiment dentaire. Pour les patients en quête d’un sourire plus blanc, les recommandations demeurent claires : consulter un chirurgien-dentiste qualifié pour des traitements utilisant le peroxyde d’hydrogène professionnel, le peroxyde de carbamide supervisé, ou les nouvelles formulations PAP. Fuir résolument les produits OTC contenant du chlorite de sodium, indépendamment de leur prix attractif ou de leurs promesses marketing, demeure la décision la plus rationnelle et la plus protectrice de la santé bucco-dentaire à long terme.